| برخی از خواص محلولها به جای ماهیت محلول ، به غلظت ذرات ماده حل شده بستگی دارد. این خواص را خواص کولیگاتیو مینامند. برای محلولهایی که شامل ماده حل شده غیر فرار هستند، این خواص عبارتند از: کاهش فشار بخار ، نزول نقطه انجماد ، صعود نقطه جوش و فشار اسمزی. |
نگاه کلی
همه ما با خواص کولیگاتیو محلولها در زندگی روزمره سرو کار داریم، بدون این که اصطلاح علمی آن را بدانیم و یا علت وقوع چنین پدیدههایی را بتوانیم توضیح دهیم. بهعنوان مثال ، در تهیه مربا و شربت به صورت علمی تجربه کردهایم که محلول آب و شکر دیرتر از
آب خالص میجوشد یا محلول آب و نمک و آب و شکر در دماهای پایینتر از دمایی که آب خالص
یخ میبندد، منجمد میشوند. وقتی در رادیاتور ماشین برای جلوگیری از انجماد آب ، ضد یخ اضافه میکنیم، از پدیده نزول نقطه انجماد استفاده کردهایم.
پدیده اسمز در بسیاری از فرآیندهای زیستی نقش اساسی دارد. مواد غذایی و زائد با عمل اسمز از میان دیواره سلولهای بافتهای حیوانی عبور داده میشوند. سلولهای خونی در محلولهای غلیظ ، آب از دست داده ، چروکیده میشوند. به همین دلیل ، باید محلولهای غذایی تزریقی به داخل سیاهرگ ، باید دقیقا طوری تنظیم شود که فشار اسمزی خون (در حدود 7.7 اتمسفر) برابر باشد.
دیواره سلولهای گیاهی و جانوری بهعنوان غشاهای نیمهتراوا عمل میکنند و در محلولهای قندی و نمکی ، آب از دست داده ، چروکیده میشوند. در زیر برخی از خواص کولیگاتیو را بررسی میکنیم.
کاهش فشار بخار
فشار بخار تعادل حلال بالای یک محلول کمتر از حلال خالص است. به تجربه دیده شده است که محلولهای آبی غلیظی مانند آب قند ، آهستهتر از آب خالص
تبخیر میشوند و این نشاندهنده کاهش فشار بخار آب بر اثر وجود ماده حل شده است. اگر غلظت ماده حل شده به حد کافی زیاد باشد، بخار موجود در اتمسفر ، مایع شده ، بعد از ورود به محلول ، آن را رقیق خواهد کرد. بررسی میزان کاهش فشار بخار نشان میدهد که این کاهش ، یک خاصیت کولیگاتیو حقیقی است و مستقیما به
غلظت ماده حل شده بستگی دارد و مستقل از ماهیت مولکولهای حل شده است.
رابطه بین فشار بخار حلال و غلظت را میتوان به این صورت بیان کرد:
P˚1 - P1 = X2 P˚1
کمیت P˚
1 - P
1 ، اختلاف بین فشار بخار حلال در مایع خالص و در محلول است و همان ، کاهش فشار بخار خواهد بود. بنابراین:
VPL =X˚2P1 (کاهش فشار بخار)
در این معادلات P
1 فشار بخار حلال روی محلول ، X
1 کسر مولی حلال در محلول و P˚
1 فشار بخار حلال خالص در همان دما ، X
2 جزء مولی ماده حل شده.
 میلیمتر است، در حالی که اندازه ذرات محلول کلوئیدی در حدود
میلیمتر است، در حالی که اندازه ذرات محلول کلوئیدی در حدود 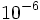 میلیمتر است.
میلیمتر است. 
















 ،
، 